ISO 9001 Beratung für Industrie und Dienstleistung
Die ISO 9001 Beratung hilft Unternehmen, ein Qualitätsmanagementsystem effizient einzuführen. Dies ist der Schlüssel, um in einem wettbewerbsorientierten Markt nachhaltig erfolgreich zu sein. Die Norm ISO 9001 definiert Anforderungen, mit denen Unternehmen ihre Prozesse optimieren, Risiken minimieren und eine kontinuierliche Verbesserung sicherstellen können – unabhängig von Branche, Größe oder Produktportfolio, deshalb ist eine ISO 9001 Beratung für ein diverses Spektrum an Kunden Vorteilhaft.
Vorteile einer ISO 9001 Beratung
- Effiziente Prozesse: Optimieren Sie Abläufe und reduzieren Sie Ressourcenaufwand.
- Höhere Kundenzufriedenheit: Erfüllen Sie Erwartungen mit gleichbleibend hoher Qualität.
- Rechtssicherheit: Halten Sie gesetzliche und behördliche Anforderungen mühelos ein.
- Wettbewerbsfähigkeit stärken: Positionieren Sie sich als zuverlässiger Partner mit internationalen Standards.
- Nachhaltige Entwicklung fördern: Verbessern Sie Ihr Unternehmen kontinuierlich.
Wie wir Sie unterstützen durch eine umfassende ISO 9001 Beratung:
Unser Ziel ist es, den Weg zur ISO 9001-Zertifizierung für Sie so einfach und effizient wie möglich zu gestalten. Wir begleiten Sie durch den gesamten Prozess – von der ersten ISO 9001 GAP-Analyse bis hin zur erfolgreichen ISO 9001 Zertifizierung. Dabei legen wir bei unserer ISO 9001 Beratung besonderen Wert auf Lösungen, die langfristig zukunftsfähig sind und nachhaltige Vorteile bieten.
Eine detaillierte Übersicht unserer Dienstleistungen finden Sie unter Leistungen, wo Sie gezielt in die einzelnen Themen eintauchen können. So erfahren Sie, wie wir Sie bei jedem Schritt optimal unterstützen, sei es bei der ISO 9001 GAP-Analyse , beim ISO 9001 Audit oder der Auswahl des passenden Dienstleisters für Ihre ISO 9001 Beratung und ISO 9001-Zertifizierung.
Ihr Weg zur ISO 9001-Zertifizierung beginnt hier
Setzen Sie mit Hopp + Flaig auf einen erfahrenen Partner für Ihre ISO 9001 Beratung und die erfolgreiche ISO 9001 Zertifizierung. Kontaktieren Sie uns, um ein kostenloses Erstgespräch zu vereinbaren. Gemeinsam machen wir Qualität zu Ihrem Wettbewerbsvorteil.
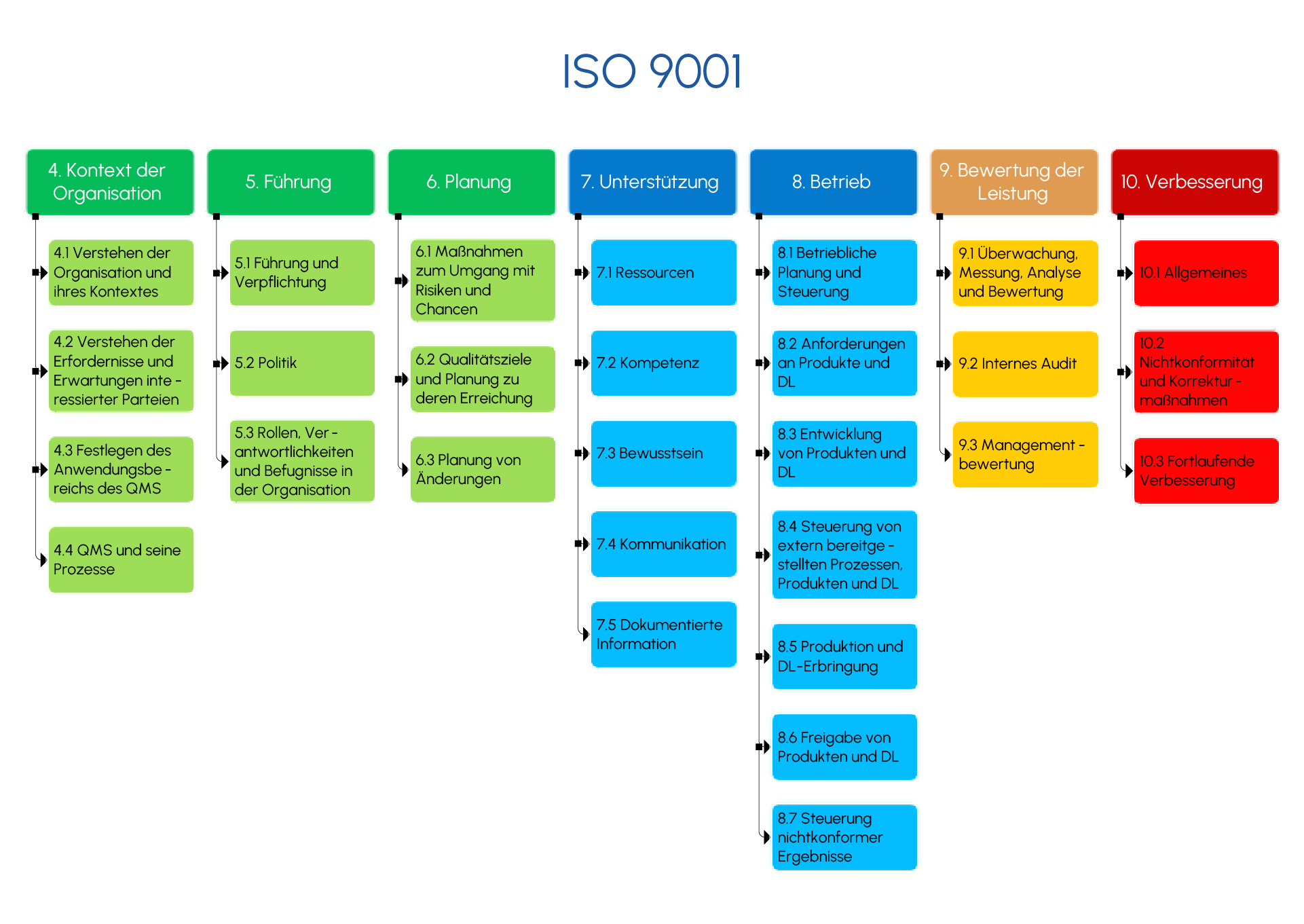
Normenanforderung
Anzahl Zertifizierungen
Deutschland
Europa
Weltweit
Anzahl Zertifizierungen
Quelle: International Organization for Standardization (ISO), ISO Survey 2023 results – number of certificates and sites per country and the number of sectors overall, veröffentlicht am 15. Januar 2025. URL: ISO/CASCO – Committee on conformity assessment.